(حل المسائل ترمودینامیک پیشرفته)
قوانین ترمودینامیک
قانون صفرم ترمودینامیک
در این قسمت بحثمان را با قانون صفرم ترمودینامیک ادامه داده و مروری بر ترمودینامیک دورۀ لیسانس خواهیم داشت.
قانون صفرم در مورد تعادل دمایی صحبت میکند و مبنای ساخت ترمومتر هم هست. یعنی کاربرد قانون صفرم ترمودینامیک را میتوانیم در ساخت ترمومتر بدانیم. در واقع، قانون صفرم میگوید که اگر دو جسم با هم در تعادل دمایی باشند و جسم دوم با جسم سومی در تعادل دمایی باشد، آنگاه جسم اول و سوم هم با همدیگر در تعادل دمایی خواهند بود و هر سه جسم با همدیگر تعادل دمایی خواهند داشت.
همانطوری که میدانید مبنای ترمومتر هم همین است. به اینصورت که در سیستم ترمومتر یک حسگر دما تعبیه میشود و دما به یک واسط انتقال مییابد. سپس ما با استفاده از این واسط میتوانیم دما را قرائت کرده و تشخیص بدهیم.
قانون اول ترمودینامیک
همانطوری که در درس اول از این مجموعه بیان کردیم، قانون اول ترمودینامیک در واقع همان قانون بقای انرژی است. برای مطالعۀ بیشتر میتوانید به قسمت “درس اول – ترمودینامیک پیشرفته” مراجعه کنید.
کاربرد قانون بقای انرژی
اگر بخواهیم اندازۀ یک مبدل حرارتی را تعیین کنیم، نیازمند این هستیم که در اطراف آن مبدل موازنۀ انرژی بنویسیم. در واقع، بدون موازنۀ انرژی این امکان برای ما وجود نخواهد داشت که اندازۀ مبدل حرارتی مورد نظرمان را تعیین کنیم یا بهعبارتی آن را سایز کنیم. همچنین، وقتی داریم یک برج تقطیر را طراحی میکنیم نیز روی هر سینی نیازمند این هستیم که موازنۀ انرژی را بنویسیم. بنابراین موازنۀ انرژی یکی از ابزارهای اساسی ما در مهندسی شیمی است.
حالا برای اینکه بتوانیم موازنۀ انرژی را بنویسیم باید آنتالپی یا انرژی داخلی جریانهای ورودی و خروجی مربوط به دستگاه مورد نظرمان را داشته باشیم. پس یکی از کاربردهای ترمودینامیک مهندسی شیمی محاسبۀ انتالپی و انرژی داخلی، و یا بهعبارت دیگر خواص ترمودینامیکی است. این مورد یکی از کاربردهای موازنۀ انرژی در مهندسی شیمی میباشد.
(حل المسائل ترمودینامیک پیشرفته)
تفاوت دیدگاه مهندسی مکانیک و مهندسی شیمی به علم ترمودینامیک
نگاهی که دوستان مهندسی مکانیک نسبت به ترمودینامیک دارند بیشتر همان ترمودینامیک کلاسیک است و خیلی روی اینکه خواص جریانها چطور محاسبه میشود، بررسی نمیکنند. ولی نگاه یک مهندس شیمی به ترمودینامیک یک مقداری با مهندس مکانیک متفاوت است. یک مهندس مکانیک اگر فرضاً بخواهد موازنۀ انرژی در اطراف یک دستگاه را بنویسد، در واقع بهدنبال این است که خواص مربوط به جریانها را با استفاده از جداول پیدا کند. ولیکن یک مهندس شیمی باید بتواند خواص جریانها را خودش محاسبه کند، و از آنجایی که جریانهای ما هم عمدتاً خالص نیستند، محاسبۀ خواص مخلوطها یکی از اساسیترین کارهایی است که بهعنوان یک مهندس شیمی باید بتوانیم آن را انجام دهیم.
(حل المسائل ترمودینامیک پیشرفته)
حالا، قانون بقای انرژی یا همان قانون اول ترمودینامیک به ما چه میگوید؟ میگوید که مجموع انرژی سیستم و محیط، یک مقدار ثابت است. وقتی صحبت از انرژی به میان میآید، باید انواع انرژی را بشناسیم.
انواع انرژی
شما با انواع انرژی در دروس مختلف برخورد داشتهاید.
انرژی جنبشی: مربوط به حرکت است که میتوانیم در اینجا انرژی جنبشی سیال را نیز تعریف کنیم که مربوط به حرکت سیال است. همچنین میتوانیم انرژی جنبشی را برای مولکولها نیز تعریف کنیم که به سرعت مولکولها بستگی دارد. در واقع ما وقتی صحبت از انرژی جنبشی میکنیم دو نوع نگاه میتوانیم داشته باشیم:
نگاه ماکروسکوپیک – نگاه میکروسکوپیک
انرژی درونی: همانطوری که بیان کردیم، نگاه ماکروسکوپیک (یا نگاه ماکرو) به سرعت سیال مربوط میشود، ولی اگر نگاه بین مولکولی داشته باشیم، انرژی جنبشی درونی به انرژی داخلی (یا درونی) ارتباط پیدا میکند.
بنابراین، برای اینکه بتوانیم برای این دو تفاوت قائل شویم، وقتی صحبت از انرژی جنبشی بین مولکولی میکنیم از عبارت “انرژی درونی” استفاده میکنیم. چون انرژی درونی است که رابطهای مستقیم با انرژی جنبشی مولکولها دارد و همچنین وابسته به دما است. یعنی هر چه دمای مولکولها بالاتر باشد، انرژی جنبشی مولکولها نیز بیشتر است. بهعبارت دیگر، مقدار انرژی درونی آنها بالاتر میشود.
انرژی درونی وابسته به سرعت مولکولها و برهمکنش بین مولکولها است. از آنجایی که ما شاید امکان اندازهگیری برهمکنشهای بین مولکولی را نداشته باشیم بهطور کلی مجموع این انرژیها را، چه انرژی مربوط به حرکت مولکولها که ناشی از دمای خودشان است و چه انرژی ناشی از برهمکنشهای بین مولکولی را کلاً “انرژی درونی” مینامیم.
پس انرژی درونی خودش شامل دو نوع انرژی است. یکی انرژی جنبشی مولکولی و یکی انرژی بین مولکولی، که مجموع اینها همان انرژی درونی است.
اما وقتی میگوییم “انرژی جنبشی” منظورمان نگاه ماکروسکوپیک و کلان است. در واقع منظورمان سرعت سیالی است که داخل سیستم ما در حال حرکت است یا به هر نحو دیگری سرعتی دارد.
انرژی پتانسیل: وقتی از انرژی پتانسیل صحبت میکنیم، منظورمان انرژی فشاری است. هر سیالی داخل سیستم، فشاری دارد که برایش انرژی پتانسیل تولید میکند.
(حل المسائل ترمودینامیک پیشرفته)
فرم سادۀ قانون اول برای یک سیستم بسته
در قانون اول ترمودینامیک گفته میشود که مقدار هر سه نوع انرژی (درونی-جنبشی-پتانسیل)، مقداری ثابت است. در واقع داریم:
![]()
و یا:
![]()
البته ما دو نوع انرژی دیگر هم داریم: “کار” و “گرما”
که تغییرات کار و گرما، هر دو باعث تغییر این انرژیها و انرژی محیط میشوند. تغییرات انرژی را با علامت ![]() نشان میدهیم.
نشان میدهیم.
تغییرات انرژی سیستم:
![]()
تغییرات انرژی محیط از طریق تبادل کار و گرما:
![]()
در واقع تغییرات انرژی محیط با انتقال کار و گرما در ارتباط است.
در این بخش، ما سیستمی را بهشکل زیر تعریف میکنیم: (و این سیستم میتواند باز یا بسته باشد و ما در اینجا فرض میکنیم که این سیستم، یک سیستم بسته است.)
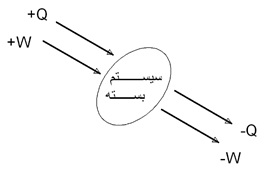
این سیستم میتواند از طریق کار و گرما با محیط در ارتباط باشد. میتواند کار بر روی آن انجام بشود، و همچنین میتواند گرما نیز به آن وارد شود (بههمین دلیل، علامت کار و گرمای ورودی به سیستم مثبت شده است). پس این سیستم میتواند با محیط تبادل کار و گرما داشته باشد.
اکنون، همانطوری که بیان شد، طبق قرارداد، اگر کار روی سیستم انجام بشود (کار وارد شده به سیستم داشته باشیم)، مقدار آن را مثبت در نظر میگیریم. و اگر گرما به سیستم وارد بشود، باز هم مقدار آن را مثبت میگیریم.
ولی اگر سیستم روی محیط کار انجام بدهد و یا تبادل گرما با محیط داشته باشد، مقدارش را منفی در نظر میگیریم (مانند شکل زیر).
بر طبق قرارداد گفته شده، در تغییرات انرژی محیط ![]() ، علامت
، علامت ![]() را منفی در نظر گرفتهایم. برای اینکه نشان بدهیم
را منفی در نظر گرفتهایم. برای اینکه نشان بدهیم ![]() از محیط خارج شده و وارد سیستم شده است. مجدداً بیان میکنیم که، همانند شکل زیر، در مورد محیط، وقتی گرما از آن خارج میشود، علامتش منفی شده است. و چون کار هم روی سیستم انجام شده و در واقع کار از محیط به سیستم منتقل گردیده و باز هم علامت آن منفی میشود.
از محیط خارج شده و وارد سیستم شده است. مجدداً بیان میکنیم که، همانند شکل زیر، در مورد محیط، وقتی گرما از آن خارج میشود، علامتش منفی شده است. و چون کار هم روی سیستم انجام شده و در واقع کار از محیط به سیستم منتقل گردیده و باز هم علامت آن منفی میشود.
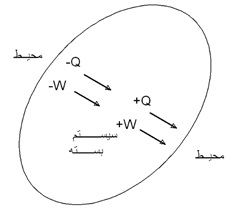
با توجه به این تعاریف فوق، جمع تغییرات انرژی سیستم و تغییرات انرژی محیط با همدیگر، یک مقدار ثابتی است. بهعبارت دیگر داریم:

در واقع، تغییرات انرژی درونی مساوی با مجموع کار و گرما میباشد. بنابراین اگر گرما و کار به سیستم وارد شوند (یعنی علامت آنها مثبت باشد) و از آنجا که تغییرات انرژی محیط با تغییرات انرژی سیستم برابر است، میتوانیم به رابطۀ زیر برسیم:
![]()
که این رابطه همان قانون اول ترمودینامیک است. اگر از تغییرات انرژی جنبشی و پتانسیل هم صرف نظر کنیم، به همان رابطۀ قانون اول در مورد سیستمهای بسته میرسیم.
![]()
این رابطه به ما میگوید که تغییرات انرژی سیستم برابر با مقدار کار و گرمای وارد شده به سیستم است.
حال اگر کار و گرما از سیستم خارج بشوند، علامت آنها نیز عوض میشود. بنابراین ما در بسیاری از موارد از علامت منفی برای کار و گرما استفاده میکنیم.
![]()
این رابطه در واقع، همان قانون بقای انرژی برای یک سیستم بسته است.
(حل المسائل ترمودینامیک پیشرفته)
از آنجا که مطالب فوق مروری بر ترمودینامیک دوره لیسانس است، برای مشاهده تمارین حل شده در این زمینه میتوانید بر روی لینهای زیر کلیک نمایید.
“تمارین سفارشی ترمودینامیک یک “
“تمارین سفارشی ترمودینامیک دو”
برای مشاهدۀ اولین بخش از این آموزش میتوانید بر روی “اینجا” کلیک کنید.