(حل المسائل ترمودینامیک پیشرفته)
اهداف کلی دورۀ ترمودینامیک پیشرفته
- بررسی ترمودینامیک مهندسی شیمی در مقطع کارشناسی
- بحث دربارۀ پیشینه نظری موضوع با جزئیات بیشتر
- معرفی برخی از ابزارهایی که بهوسیله آنها میتوان خواص مولکولی را به خواص ماکروسکوپی مرتبط کرد
- بحث در مورد کاربردها، در زمینههای ارزیابی خواص فیزیکی، همبستگی و پیشبینی سیستمهای تعادل
مطالب مربوط به ترمودینامیک پیشرفته را با قانون اول ترمودینامیک شروع میکنیم.
قانون اول ترمودینامیک چیست و چه کاربردی دارد؟
قانون اول ترمودینامیک در واقع، قانون بقای انرژی است. از قانون بقای انرژی در انواع موازنههای انرژی مثل انتقال حرارت استفاده میکنیم. آیا در سیالات هم کاربرد دارد؟ بله. در مکانیک سیالات هم در مبحث معادلۀ برنولی از آن استفاده میکنیم. در واقع، قانون بقای انرژی برای یک سیستم بسته چنین است:
![]()
که اگر سیستم، یک سیستم باز باشد، قانون اول ترمودینامیک بدین صورت نوشته میشود:
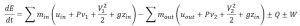
که ![]() نماد انرژی،
نماد انرژی، ![]() سرعت و
سرعت و ![]() حجم مخصوص است.
حجم مخصوص است.
اگر ما یک سیستم پایدار یا ![]() را داشته باشیم و تغییرات با زمان نداشته باشیم،
را داشته باشیم و تغییرات با زمان نداشته باشیم،
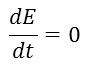
و در این معادله اگر دماها تغییری نکند، انرژیهای داخلی هم تغییر نخواهند کرد. یعنی:
![]()
چون انرژی داخلی برای گاز ایدهآل تابعی از دما است، بنابراین داریم:
![]()
بعد از ساده کردن رابطۀ فوق، آنچه که باقی میماند، در حقیقت معادلۀ برنولی خواهد بود.

میدانیم که ![]() یا حجم مخصوص عکس چگالی است.
یا حجم مخصوص عکس چگالی است.
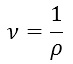
بنابراین:

و این همان شکلی میشود که معادلۀ برنولی را به همان شکل دیدهایم. اگر تبادل گرما نداشته باشیم:
![]()
کار هم میتواند مربوط به کار پمپ یا کار کمپرسور باشد. علامت مثبت نشاندهندۀ آن است که کار یا گرما وارد سیستم میشود و اگر علامت منفی باشد یعنی کار و گرما از سیستم خارج میشود، و در واقع سیستم کار انجام میدهد.
پس متوجه شدیم که موازنۀ انرژی چه کاربردهای مهمی دارد.
(حل المسائل ترمودینامیک پیشرفته)
توابع حالت در مقابل توابع مسیر
در ترمودینامیک 1 گفتیم که دو نوع تابع داریم: ![]() و
و ![]() .
.
توابع حالت، از ویژگیهای سیستم هستند:
– خواصی که مواد میتوانند داشته باشند. بهعنوان مثال T، P، S، U، V، H، G
توابع مسیر، از ویژگیهای فرآیند هستند:
– ویژگیهایی که فقط یک فرآیند میتواند داشته باشد به عنوان مثال Q ، W
توابع حالت دارای دیفرانسیل کامل هستند (مقدار آنها بستگی به وضعیت فعلی دارد).
توابع مسیر دارای دیفرانسیل غیرکامل هستند (مقدار آنها بستگی به نحوۀ ایجاد تغییر دارد).
برخی از خواص ترمودینامیکی تابع حالتاند و برخی دیگر تابع مسیرند.
(حل المسائل ترمودینامیک پیشرفته)
تابع حالت چیست؟
وقتی ما میگوییم تابع حالت، منظورمان این است که آن خاصیت ترمودینامیکی فقط به آن حالت ترمودینامیکی بستگی دارد؛ و به این بستگی ندارد که چطور به آن حالت ترمودینامیکی رسیده است.
حالت ترمودینامیکی چیست؟ چه چیزی حالت ترمودینامیکی را تعیین میکند؟
در واقع سؤال این است: چه وقت حالت ترمودینامیکی مشخص میشود و به چه چیزی بستگی دارد؟
حالت ترمودینامیکی وقتی مشخص میشود که درجۀ آزادی برابر با صفر شود.
![]()
(حل المسائل ترمودینامیک پیشرفته)
درجۀ آزادی یعنی چه؟
درجۀ آزادی یعنی تعداد مجهولات منهای تعداد معادلات یا معلومات. پس داریم:
![]()
بنابراین وقتی ما میگوییم درجۀ آزادی صفر است یعنی تعداد مجهولاتمان و تعداد معادلاتمان با همدیگر برابر است. پس درجۀ آزادی چنین میشود:
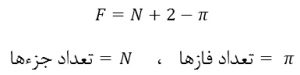
با استفاده از این رابطه میتوانیم درجۀ آزادی را تعیین کنیم. مثلاً اگر ما مادۀ خالص داشته باشیم:
![]()
یعنی برحسب تعداد فازها داریم:
![]()
یعنی اگر مادۀ خالص داشته باشیم که تک فاز باشد، یعنی مثلاً مایع باشد، یا بخار باشد، یا جامد باشد، وقتی حالت ترمودینامیکیاش مشخص میشود (یعنی همۀ مقادیر ![]() و ظرفیت گرمایی ویژهاش در فشار ثابت و در حجم ثابت برایش معلوم میشود)، که حداکثر دو متغیر را برایش معلوم کنیم. به عبارت دیگر، وقتی همۀ خواص یک مادۀ خالص در حالت تکفازی معلوم میشود که دو متغیر از کلیۀ خواص شدتی را مشخص کنیم.
و ظرفیت گرمایی ویژهاش در فشار ثابت و در حجم ثابت برایش معلوم میشود)، که حداکثر دو متغیر را برایش معلوم کنیم. به عبارت دیگر، وقتی همۀ خواص یک مادۀ خالص در حالت تکفازی معلوم میشود که دو متغیر از کلیۀ خواص شدتی را مشخص کنیم.
![]()
مثلاً مشخص کنیم که مقدار آنتالپیاش و مقدار حجم مخصوصاش چقدر است. یا مثلاً مشخص کنیم که دما و فشارش چقدر است.
فرقی هم نمیکند که کدام را مشخص کنیم. اگر دو خاصیت از بین کلیۀ خواص را معلوم کنیم حالت فازی ماده معلوم میشود. یعنی در واقع حالتش مشخص میشود. پس وقتی میگوییم یک تابعی، تابع حالت است یعنی این تابع فقط تابع این است که حالت مادۀ ما فیکس شده باشد.
معمولاً از بین خواص مختلف برای مشخص کردن حالت، دما و فشار را بهعنوان متغیرهای حالت در نظر میگیریم و میگوییم در دما و فشار مشخص.
حال اگر مخلوط ما خالص نباشد، علاوه بر دما و فشار، کامپوزیشن ![]() هم در اینجا اضافه میشود. با استفاده از قانون درجۀ آزادی یا قاعدۀ فاز باید مشخص کنیم که چه چیزهایی را باید معلوم کنیم تا حالت مادۀ ما مشخص شود.
هم در اینجا اضافه میشود. با استفاده از قانون درجۀ آزادی یا قاعدۀ فاز باید مشخص کنیم که چه چیزهایی را باید معلوم کنیم تا حالت مادۀ ما مشخص شود.
پس حالا وقتی میگوییم تابع ما، تابع حالت است یعنی با مشخص شدن این متغیرهای حالت، وضعیت مادۀ ما کاملاً مشخص میشود. وضعیت ماده دیگر بستگی به این ندارد که ما چطوری به این حالت رسیدهایم. چطوری به این دما و فشار رسیدهایم. بهطور مثال فرض میکنیم که مادۀ خالص داریم. اگر این ماده را از دمای ![]() و فشار
و فشار ![]() به دمای
به دمای ![]() و فشار
و فشار ![]() برسانیم، فرقی نمیکند که ما چطوری از
برسانیم، فرقی نمیکند که ما چطوری از ![]() و
و ![]() به
به ![]() و
و ![]() رسیدهایم. در واقع به مسیر ارتباطی ندارد. فقط به حالت بستگی دارد، حالت اولیه و حالت ثانویه.
رسیدهایم. در واقع به مسیر ارتباطی ندارد. فقط به حالت بستگی دارد، حالت اولیه و حالت ثانویه.
برخی از توابع هستند که تابع مسیرند. یعنی ما برای آنها نمیتوانیم بر حسب حالتشان مقدار بدهیم. اگر به جداول ترمودینامیکی مراجعه کنید متوجه میشوید که در جداول ترمودینامیکی بر حسب دما و فشار، حجم مخصوص، آنتروپی، آنتالپی و انرژی آزاد گیبس و … همۀ اینها مشخص شدهاند. یعنی گفته شده که در شرایط مختلف مقادیرشان چقدر است. اما برای کار و گرما جدولی نداریم. چون کار و گرما تابع حالت نیستند. و لیکن ما میتوانیم بگوییم در این دما و فشار و کامپوزیشن، مقدار آنتالپی چقدر است.
اگر ما برای خاصیتی بتوانیم در دما و فشار و کامپوزیشن، بگوییم مقدارش چقدر است، آنوقت دیگر آن تابع، تابع حالت است؛ و اگر نتوانیم مقدار را مشخص کنیم، تابع مسیر میشود.
حالا در مورد آب خالص، اگر بگوییم آب در 20 درجۀ سانتیگراد، حالتاش مشخص نمیشود. شما باید بپرسید فشار آب در 20 درجۀ سانتیگراد چقدر است؟
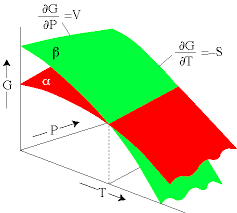
در نمودار فازی، اگر نمودار فشار بر حسب دما را برای یک مادۀ خالص ترسیم کنیم، چنین میشود:
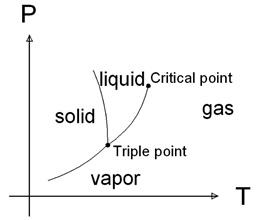
در این نمودار اگر بخواهیم حالت یک مادهای را (بجز نقاط روی منحنی) مشخص کنیم باید حتماً دو تا مختصات داشته باشیم، یعنی دما و فشار. اگر شرایط ماده بهگونهای باشد که بر روی منحنی تعادل بخار – مایع قرار داشته باشد، کافی است بگوییم بخار اشباع ![]() در دمای معلوم. دیگر لازم نیست فشار را مشخص کنیم.
در دمای معلوم. دیگر لازم نیست فشار را مشخص کنیم.
پس وقتیکه ![]() است، فقط لازم است که یک متغیر را مشخص کنیم، یا دما، یا فشار. اگر مشخصات ماده بر روی نقطۀ سه گانه
است، فقط لازم است که یک متغیر را مشخص کنیم، یا دما، یا فشار. اگر مشخصات ماده بر روی نقطۀ سه گانه ![]() قرار داشته باشد، دیگر نیازی نیست که هیچ متغیری را مشخص کنیم. مختصات نقطۀ سه گانه کاملاً مشخص است. این مفهوم “درجۀ آزادی” و مفهوم “حالت” است. وقتی ما میگوییم “حالت”، میخواهیم مشخص کنیم که مادهمان دقیقاً در چه وضعیتی قرار دارد.
قرار داشته باشد، دیگر نیازی نیست که هیچ متغیری را مشخص کنیم. مختصات نقطۀ سه گانه کاملاً مشخص است. این مفهوم “درجۀ آزادی” و مفهوم “حالت” است. وقتی ما میگوییم “حالت”، میخواهیم مشخص کنیم که مادهمان دقیقاً در چه وضعیتی قرار دارد.
(حل المسائل ترمودینامیک پیشرفته)
اکنون میخواهیم بدانیم که کاربرد تابع حالت در کجاست.
ویژگی تابع حالت:
ویژگی تابع حالت این است که دارای دیفرانسیل کامل میباشد. این مطلب بسیار مهم است. اینکه تابع حالت دارای دیفرانسیل کامل است یعنی چه؟
یعنی اگر فرض کنیم که یک تابعی داریم به نام ![]() ، که متغیرهایش
، که متغیرهایش ![]() و
و ![]() و
و ![]() است(این متغیرها میتوانند بیشتر هم باشند) میتوانیم چنین بنویسیم:
است(این متغیرها میتوانند بیشتر هم باشند) میتوانیم چنین بنویسیم:
![]()
در اینجا میتوانیم ![]() را بهجای
را بهجای ![]() ،
، ![]() را بهجای
را بهجای ![]() ،
، ![]() را بهجای
را بهجای ![]() ،
، ![]() را بهجای
را بهجای ![]() قرار دهیم. یعنی یک تابع به نام آنتالپی داریم که تابع دما، فشار و کامپوزیشن است.
قرار دهیم. یعنی یک تابع به نام آنتالپی داریم که تابع دما، فشار و کامپوزیشن است.
![]()
اگر تابع ![]() دیفرانسیل کامل باشد، یعنی ما میتوانیم
دیفرانسیل کامل باشد، یعنی ما میتوانیم ![]() را بدینصورت بنویسیم:
را بدینصورت بنویسیم:
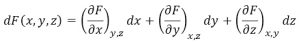
اگر متغیرهای دیگری هم داشتیم میتوانستیم در اینجا آنها را نیز بنویسیم.
پس ما تابعی را که دیفرانسیل کامل باشد میتوانیم به اینصورت آن را تفکیک کنیم. برای آنتالپی نیز میتوانیم این کار را انجام دهیم و این برای ما خیلی مهم است که بتوانیم خواص ترمودینامیکی را به اینصورت بنویسیم. مثلاض در مورد آنتالپی داریم:
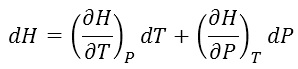
ما میتوانیم مقدار آنتالپی را در فشار و دمای معلوم با استفاده از مقدار آنتالپی در مقدار مرجع آن بهدست بیاوریم. یعنی میتوانیم در فشار ثابت، دما را از دمای مرجع تا دمای موردنظر تغییر داده و سپس فشار را در دمای ثابت از فشار مرجع تا فشار موردنظر تغییر دهیم.
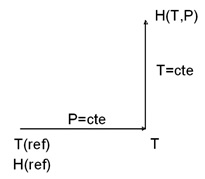
اگر ما این کار را بتوانیم انجام دهیم میتوانیم مستقلاً انتگرالهای زیر را نیز بهدست آوریم و آنتالپی را در هر دما و فشاری که لازم داریم محاسبه کنیم.
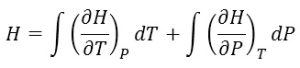
و این رابطه بسیار مهم است. بههمین دلیل برایمان مهم است که تابع حالت را تعریف کنیم. اگر چه ما ![]() و
و ![]() برایمان ملموس است ولی بهجای
برایمان ملموس است ولی بهجای ![]() و
و![]() ،
، ![]() را تعریف کردیم که یک تابع حالت است.
را تعریف کردیم که یک تابع حالت است. ![]() و
و![]() تابع حالت نیستند.
تابع حالت نیستند.
![]()
ویژگی دیگری که تابع حالت دارد این است که ترتیب مشتقگیری در تابع حالت اهمیتی ندارد. یعنی:
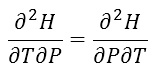
بنابراین میتوانیم به هر ترتیبی که دلخواهمان بود مشتق بگیریم. ترتیب مشتقگیری برای ما اهمیتی ندارد.
(حل المسائل ترمودینامیک پیشرفته)
در مطالب فوق تفاوت بین تابع حالت و تابع مسیر و ویژگیهای تابع حالت بیان شد.
ویژگیهای تابع حالت بهطور خلاصه:
تابع حالت دارای دو ویژگی است. یکی اینکه تابع حالت دیفرانسیل کامل دارد و چون دیفرانسیل کامل دارد ما میتوانیم آن را بهصورت مشتق جزئی بنویسیم. همچنین میتوانیم در طول مسیر فرآیند از آن انتگرال بگیریم که این مطلب بسیار مهم است.
نکتۀ دوم اینکه میتوانیم به هر نحوی که خواستیم از آن مشتق بگیریم و ترتیب مشتقگیری برای ما اهمیتی ندارد و نتیجۀ نهاییاش مهم میباشد.
(حل المسائل ترمودینامیک پیشرفته)
برای مشاهدۀ حل مسائل مرتبط با این مبحث میتوانید بر روی لینکهای زیر کلیک کنید.
“مسئله 38- محاسبه انتقال حرارت در طی فرآیند تراکم در کمپرسور“
“مسئله 53 – محاسبه S∆ و H∆ برای گاز خالص با استفاده از معادله حالت PR“
برای مشاهدۀ ادامۀ این آموزش میتوانید بر روی “اینجا” کلیک کنید.